Synthèse de la publication
Effective inhibition of Th17/Th22 pathway in 2D and 3D human models of psoriasis by celastrol enriched plant cell culture extract
Objectif
Evaluer l’effet immunomodulateur du Célastrol dans des modèles in vitro d’inflammation de type psoriasique.
Le Célastrol est un triterpène produit in vitro à partir de culture de cellules végétales de Tripterygium Wilfordii (technique brevetée de l'unité de biotechnologie du Centre de Recherche Pierre Fabre).
Méthodologie
Préincubation des lymphocytes humains T CD4+ (hCD4), kératinocytes humains normaux (NHEK), micro-épiderme et épiderme humain reconstruit (RHE) avec du Célastrol et des contrôles de référence.
Critères d'évaluation
Quantification des biomarqueurs du psoriasis par la méthode immuno-enzymatique ELISA.
Résultats
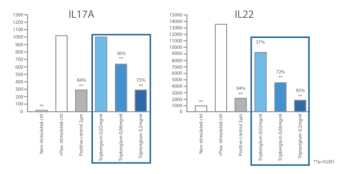
- LYMPHOCYTES T CD4+
Le Célastrol inhibe la production des cytokines IL-17A et IL-22 de façon dose-dépendante
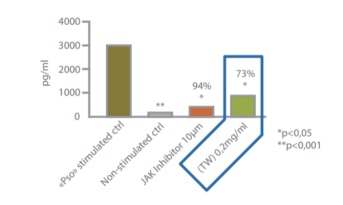
- EPIDERME HUMAIN RECONSTRUIT :
Le Célastrol inhibe la production du médiateur pro-inflammatoire IL-8
Conclusion
Le Célastrol a la capacité de moduler l’inflammation de type TH17/TH22 en agissant sur 2 cibles : les lymphocytes T et les kératinocytes.
Nos autres publications à ce sujet
Vous souhaitez poursuivre votre lecture ?
Cet accès est réservé aux professionnels, inscrits sur Pierre Fabre For Med.
Pour accéder à l’intégralité du contenu, veuillez vous inscrire ou vous connecter si vous possédez déjà un compte.
